¿Son las ciudades seres vivos? Nadie pone en duda el hecho de que una planta está tan viva como un insecto o un humano. A pesar de que la definición de ser vivo puede resultar polémica, por lo general se considera que todo ser que posee cierto nivel de organización, un metabolismo, mantiene una homeostasis determinada, es capaz de crecer y reproducirse, responde ante los estímulos y evoluciona (Khan Academy, s.f.). Los niveles de organización son evidentes en el caso de una mosca: está organizada en sistemas con funciones generales, compuestos por órganos que se coordinan para asegurar el funcionamiento de los sistemas, que contienen tejidos hechos por células que pueden efectuar diferentes funciones en función de su especialización, determinada por los genes expresados y la presencia de diferentes moléculas. ¿Acaso una ciudad no tiene una organización similar, con diferentes instituciones y diferentes oficios que se coordinan y se complementan entre sí? A su vez, todos estos dependen del funcionamiento coordinado de seres humanos o máquinas que los mantienen, que a su vez se componen de un sinfín de niveles de organización. De la misma forma, podría considerarse que la transformación de materia prima en productos útiles, o el trabajo realizado por las industrias energéticas o encargadas de asegurar la disponibilidad de agua podrían constituir su metabolismo. La homeostasis o la regulación que permite el mantenimiento del equilibrio de una ciudad puede encontrarse en múltiples ejemplos, como la temperatura cíclica y más o menos estabilizada, o incluso la limpieza diaria de la misma. En lo que concierne al crecimiento y la reproducción, no es difícil imaginar una ciudad en plena expansión de territorio, ya que es algo a lo que tiende toda población que funciona bien. La respuesta ante estímulos es igualmente posible: cuando una catástrofe natural ocurre, los desastres materiales son progresivamente restaurados o reparados. La evolución de las ciudades es también un hecho. Tan solo hay que tratar de imaginar una ciudad hace 20 siglos y compararla con la imagen de una actual.
Reflexionar sobre los diferentes niveles de organización (molécula, organismo, ciudad, país…) siempre es interesante. Y este ejercicio de pensamiento puede hacerse en los dos sentidos. Este artículo se centra en un nivel de organización celular y molecular. Las neuronas son cuerpos organizados compuestos por diferentes moléculas. Cuando las moléculas empiezan a fallar, las células experimentan sus consecuencias. Cuando muchas células experimentan sus consecuencias, es posible que tejidos e incluso órganos comiencen a funcionar de forma deficiente. Y cuando esto ocurre, los problemas se hacen visible a ojos del ser humano.
¿Qué ocurre a nivel cerebral?
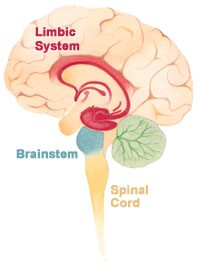
La demencia con cuerpos de Lewy es la tercera enfermedad neurodegenerativa más común tan solo después del Alzheimer y del Parkinson. La mayoría de los pacientes de demencia con cuerpos de Lewy (DCL) presentan una pérdida de neuronas dopaminérgicas en la sustancia negra, una región perteneciente a los ganglios basales (ver Figura 1). Asimismo, la patología afecta de forma considerable a nivel del neocórtex (capa más externa del cerebro, también conocida como corteza cerebral) y del sistema límbico (ver Figura 2). El neocórtex está implicado en funciones superiores como la memoria, la orientación espacial y el lenguaje (Wikipedia contributors, 2020a). El sistema límbico, por su parte, se asocia a funciones como la emoción, la memoria a largo plazo y la olfacción (Wikipedia contributors, 2020b).

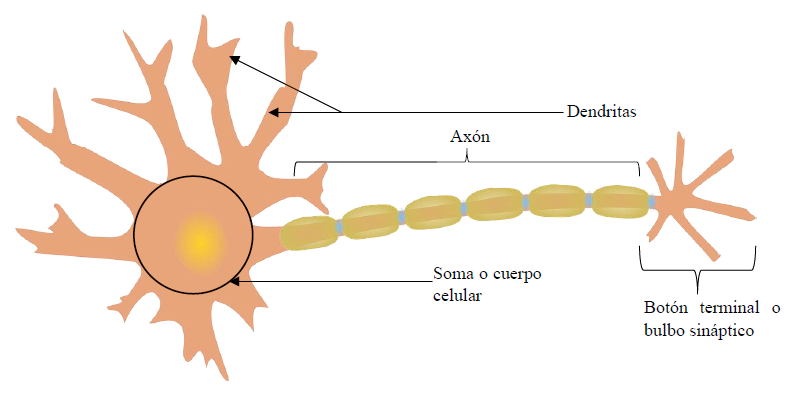
Desde un punto de vista macroscópico, los cerebros de las personas con DCL manifiestan una atrofia generalizada, característica en común con los pacientes de Alzheimer. Desde un punto de vista microscópico, la DCL se caracteriza por la acumulación de la proteína α-sinucleína en las neuronas. Las acumulaciones de α-sinucleína en el soma (ver Figura 3) son conocidas como cuerpos de Lewy y dan el nombre a este tipo de demencias. A los agregados de dicha proteína en las dendritas o el axón neuronal se los conoce como neuritas de Lewy. Según Outeiro et al. (2019), en un contexto celular patológico la proteína α-sinucleína cambia de conformación y adquiere una estructura conocida como hojas beta. Esta estructura podría favorecer la agregación. La expansión de los agregados a lo largo del cerebro podría seguir un mecanismo de tipo priónico (Outeiro et al., 2019). Se conoce como prión a una proteína que posee una forma que favorece la agregación. Por lo general, se asocia la agregación priónica a un fenómeno aberrante, aunque para ciertos vivos como el champiñón Podospora anserina es un mecanismo no patológico. El modelo de expansión priónica conocido como asistencia del modelo propone que la mera interacción de una proteína priónica con una proteína no priónica es suficiente para que esta última adquiera la conformación aberrante (Brundin, Melki & Kopito, 2010). Los priones pueden igualmente transmitirse de una célula a otra por mecanismos de endocitosis (formación de una vesícula en la membrana celular e internalización de esta) así como mediante contacto directo desde el axón a través del axón de una neurona y las dendritas de otra (Brundin, Melki & Kopito, 2010). La manifestación de la agregación de α-sinucleína comienza a manifestarse, por lo general, en el sistema límbico y en las áreas neocorticales, donde su presencia se asocia al déficit cognitivo característico de la enfermedad (aunque no a su gravedad, como se explica más adelante). Asimismo, la proteína α-sinucleína puede experimentar modificaciones postraduccionales (es decir, modificaciones estructurales que tienen lugar después de su síntesis) consistentes en la agregación de grupos moleculares que pueden tener una influencia en su función. Entre las modificaciones postraduccionales que la α-sinucleína puede manifestar se encuentra la fosforilación. Se ha constatado que los pacientes de DCL presentan una mayor cantidad de dicha proteína fosforilada que de proteína no modificada. Además, se han detectado estas formas modificadas de α-sinucleína en los cuerpos y las neuritas de Lewy (Outeiro et al., 2019). Estos datos llevan a pensar que la fosforilación juega un papel importante en la enfermedad, aunque todavía no se sabe el lugar que ocupa. Se cree que otros factores, como la presencia de síntomas típicos de Alzheimer o los genes, pueden tener una influencia sobre el nivel de agregación. En efecto, ciertas áreas presentan, además de los cuerpos o neuritas de Lewy, signos patológicos típicos del Alzheimer como placas ß-amiloide y ovillos neurofibrilares de la proteína tau. Se cree que estos marcadores pueden contribuir en el mecanismo de agregación de α-sinucleína en el neocórtex (Outeiro et al., 2019). En cualquier caso, el fenómeno de la agregación en esta enfermedad es bastante complejo: diferentes regiones cerebrales parecen ser más vulnerables que otras, se ha detectado la presencia de agregados en el sistema nervioso periférico (Outeiro et al., 2019), e incluso en diferentes sistemas como el cardiovascular, el endocrino y el respiratorio (Beach et al., 2010).
A pesar de los descubrimientos sobre las características macroscópicas y microscópicas de la DCL en el sistema nervioso, los ensayos clínicos no encuentran correlaciones entre la densidad de cuerpos de Lewy y factores como la edad de aparición de la enfermedad, su duración o la gravedad de los síntomas. Además, en la actualidad no está claro si los cuerpos de Lewy constituyen un evento patológico con consecuencias negativas sobre la supervivencia neuronal, o tan solo son una consecuencia neuroprotectora de otro evento patológico en el contexto de la enfermedad (Outeiro et al. 2019). La búsqueda de mejores predictores es necesaria, y el papel de los agregados de α-sinucleína debe ser estudiado con más profundidad.
Mecanismos moleculares de aparición de los cuerpos de Lewy
A pesar de que su papel en la demencia de cuerpos de Lewy no está del todo claro, la agregación de α-sinucleína es un evento central en esta patología. La agregación de esta proteína comienza por un proceso conocido como nucleación, en el que diferentes monómeros (una unidad de proteína) interaccionan formando oligómeros (agrupaciones de varias proteínas). Esta etapa es relativamente lenta, pero dado que las estructuras formadas son demasiado inestables, estas tienden a estabilizarse durante la etapa de elongación formando agrupaciones de oligómeros a una velocidad mucho más importante. La agregación de oligómeros da lugar a configuraciones estructurales más estables que continúan a adherirse hasta lograr una fibrilación, estado de elevada agregación (Outeiro et al., 2019). Una vez los agregados de α-sinucleína formados, estos se dispersan entre las neuronas mediante la inclusión de más α-sinucleína intacta, como se explica más arriba. Las regiones cerebrales que no presentan α-sinucleína en abundancia no dan lugar a la agregación, puesto que la fase de nucleación necesita una gran presencia de la proteína para iniciar este proceso (Outeiro et al., 2019).
En conclusión, se ha avanzado bastante en la comprensión de los mecanismos de agregación, que se relacionan de alguna forma con la toxicidad neuronal y los síntomas de la DCL. No obstante, su papel exacto sigue siendo una incógnita.
¿Existe un tratamiento para la demencia con cuerpos de Lewy?
En la actualidad no existe ningún tratamiento para curar la demencia con cuerpos de Lewy. La medicación actual se centra en el alivio sintomático, y utiliza fármacos destinados originalmente a otras enfermedades como el Parkinson o el Alzheimer (Lee, Cummings, Decourt, Leverenz & Sabbagh, 2019).
Durante mucho tiempo, los ensayos clínicos se han centrado en el alivio de síntomas puntuales como el déficit cognitivo, las alucinaciones y el trastorno del sueño REM. La presencia de síntomas tan abundantes y variados dificulta la consecución de un fármaco único capaz de abarcar la totalidad de la enfermedad. No obstante, en la actualidad, además de los sintomáticos se han desarrollado ensayos clínicos de tratamientos que modifican la enfermedad (del inglés disease modifying therapies) y encajan más con la definición de cura. No obstante, ninguno de estos últimos ha dado resultados eficaces hoy en día. Sin embargo, dos agentes moleculares parecen prometedores: pimavanserina y zonisamida (Lee, Cummings, Decourt, Leverenz & Sabbagh, 2019). Uno de los motivos por el que todavía no se han desarrollado tratamientos es la subestimación de la gravedad de esta enfermedad neurodegenerativa, o la poca importancia que se le ha dado en el terreno clínico. Un dato ilustrativo de este hecho es que en la actualidad 8 agentes terapéuticos potenciales para la DCL están siendo estudiados, 16 veces menos que los 132 agentes para la enfermedad de Alzheimer (Lee, Cummings, Decourt, Leverenz & Sabbagh, 2019).
Las vías de acción futuras deben centrarse por una parte en el desarrollo de biomarcadores fiables que permitan compensar el problemático infradiagnóstico actual y dar lugar a diagnósticos más precoces, lo que facilitaría la participación en los ensayos clínicos y mejoraría la eficacia de los tratamientos. Por otra parte, es necesario encontrar nuevas dianas moleculares para el desarrollo de terapias específicas para la demencia con cuerpos de Lewy (Lee, Cummings, Decourt, Leverenz & Sabbagh, 2019).
Mensaje para llevarse a casa
La demencia con cuerpos de Lewy es una de las enfermedades neurodegenerativas más frecuentes. Su principal característica es la aparición cuerpos y neuritas de Lewy (agregados de la proteína α-sinucleína) y la degeneración de las neuronas dopaminérgicas de la sustancia negra (en los ganglios basales). La presencia de los cuerpos de Lewy no se limita al sistema nervioso, pero la enfermedad se asocia a la agregación en áreas cerebrales como el neocórtex y el sistema límbico. La agregación es el resultado de un proceso de nucleación de monómeros de proteína y de elongación de oligómeros de esta, formando estructuras fibrilares que podrían resultar tóxicas para la célula nerviosa, o bien ser el resultado de la toxicidad originada por otros agentes. Una hipótesis para explicar la expansión de las agregaciones de α-sinucleína propone un mecanismo de tipo priónico. En la actualidad no existe ninguna cura para la enfermedad, puesto que el diagnóstico es difícil a causa de la falta de marcadores fiables, los ensayos clínicos son escasos y la enfermedad es de una gran complejidad sintomática.
Beach, T. G., Adler, C. H., Sue, L. I., Vedders, L., Lue, L., White III, C. L., … Walker, D. G. (2010). Multi-organ distribution of phosphorylated α-synuclein histopathology in subjects with Lewy body disorders. Acta Neuropathologica, 119(6), 689–702. Fuente
Brundin, P., Melki, R., & Kopito, R. (2010). Prion-like transmission of protein aggregates in neurodegenerative diseases. Nature Reviews Molecular Cell Biology, 11(4), 301–307. Fuente
Khan Academy. (s.f.). What is life? Recuperado 1 marzo, 2020, de Fuente
Lee, G., Cummings, J., Decourt, B., Leverenz, J. B., & Sabbagh, M. N. (2019). Clinical drug development for dementia with Lewy bodies: past and present. Expert Opinion on Investigational Drugs, 28(11), 951–965. Fuente
Outeiro, T. F., Koss, D. J., Erskine, D., Walker, L., Kurzawa-Akanbi, M., Burn, D., … McKeith, I. (2019). Dementia with Lewy bodies: an update and outlook. Molecular Neurodegeneration, 14(1). Fuente
Wikipedia contributors. (2020a, 16 febrero). Neocortex. Recuperado 29 febrero, 2020, de Fuente
Wikipedia contributors. (2020b, 25 febrero). Limbic system. Recuperado 29 febrero, 2020, de Fuente